QdengaTM-vaccinen indgives som to doser a 0,5 ml med tre måneders mellemrum 1
Dosis 1:
0,5 ml
Administreres ved
måned 0 (dag 1)
Dosis 2:
0,5 ml
Administreres ved
måned 3 (dag 91)
Fuld vaccineeffekt
Opnås 1
måned efter anden
dosis (dag 121)
Beskyt rejsende ved at tilbyde en vaccine i god tid inden deres rejse
Rejsende bør vaccineres med to doser QdengaTM-vaccine med tre måneders mellemrum 1

QdengaTM er indiceret til forebyggelse af denguefeber forårsaget af enhver af de fire denguevirus serotyper hos personer i alderen 4 år og derover 1
Opbevar QdengaTM ved 2-8 °C inden brug; må ikke nedfryses.
Holdbarhed: 18 måneder 1
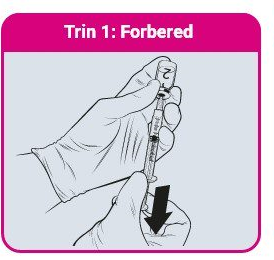
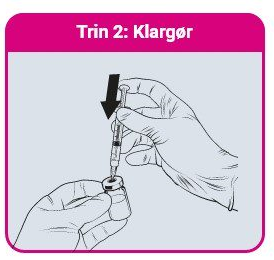
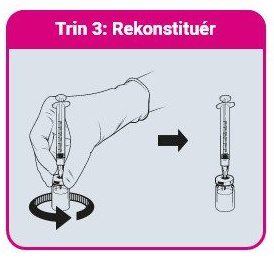
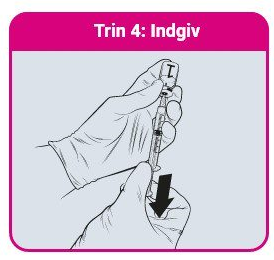




- Indgiv altid QdengaTM i henhold til den godkendte produktinformation
- QdengaTM består af pulver og solvens til injektionsvæske i forfyldt sprøjte. 1
- QdengaTM skal rekonstitueres med solvensen inden administration og anvendes med det samme efter rekonstitution 1
- Efter rekonstition skal QdengaTM anvendes inden to timer. 1
- QdengaTM skal administreres ved subkutan injektion, helst i deltamusklen i overarmen 1
- Behovet for en boosterdosis er ikke klarlagt 1
- Anbefalet nålstørrelse er 23G (trin 1-3). Anbefalet nålstørrelse til vaccineadministration er 25G (trin 4).
Udvikling
Takeda har mere end 70 års erfaring inden for udvikling og fremstilling af vacciner 2
QdengaTM er udviklet og fremstillet i overensstemmelse med cGMP-reglerne og de gældende regulatoriske krav 3,4
DEN-2-virus er blevet isoleret fra naturen og svækket. Efterfølgende er de andre kimæriske vira DEN-1, DEN-3 og DEN-4 blevet udviklet ved hjælp af rekombinante teknikker under anvendelse af den svækkede DEN-2-virus 4
DENV-2-stammen svækkes, og ved hjælp af rekombinante teknikker dannes de andre 3 kimæriske vira ved at indsætte prM- og E-proteingenerne fra DENV-1, -3 og -4 i DENV-2's genestiske basis 3
Andre ikkeaktive ingredienser, herunder stabilisatorer, tilsættes for at muliggøre en levedygtig formulering 3
Den enkelte levende, svækkede, tetravalente formulerings kvalitet og styrke (dvs. biologiske aktivitet) tjekkes for at sikre det enkelte produkts kvalitet, integritet og sikkerhed
I hvilke lande er Qdenga tilgængelig?
Vil din patient have anden dosis i et andet land - eksempelvis på rejsemålet?


- [SPC] QdengaTM Summary of Product Characteristics (12/2022)
- [TAKPR] Therapeutic Focus. Vaccines. Takeda Pharmaceutical Company Limited. [accessed 05.2021]. Available from:
https://www.takeda.com/science/areas-of-focus/vaccines/ - [OSO15] Osorio JE, Partidos CD, Wallace D, Stinchcomb DT. Development of a recombinant, chimeric tetravalent
dengue vaccine candidate. Vaccine. 2015;33(50):7112-20. - [HUA13] Huang CY, Kinney RM, Livengood JA, Bolling B, Arguello JJ, Luy BE, et al. Genetic and phenotypic
characterization of manufacturing seeds for a tetravalent dengue vaccine (DENVax). PLoS Negl Trop Dis.
2013;7(5):e2243.
cGMP = aktuel god fremstillingspraksis, DENV = denguevirus.

